

支气管扩张、慢性气道炎症、肿瘤转移等众多难治性疾病背后,长期存在一条被忽视的共同致病通路。组织蛋白酶C(Cathepsin C,又称:二肽基肽酶I即:DPP1)作为上游核心蛋白酶,如同“总开关”般激活中性粒细胞弹性蛋白酶、蛋白酶3等关键炎症效应分子,驱动组织损伤、气道重塑与肿瘤微环境形成,成为连接炎症与转移的关键节点。
随着首款CTSC抑制剂布索卡替成功获批上市,这条沉寂多年的通路正式迈入临床兑现期。从靶点机制、药物研发到全球管线竞速,CTSC抑制剂正以“源头阻断”的独特优势,为呼吸、自免炎症等未满足临床需求打开全新治疗维度。本文深度拆解这一前沿靶点,全景呈现CTSC抑制剂的研发格局与产业未来。
CTSC核心概览:
免疫激活与组织重塑的关键蛋白酶
组织蛋白酶C,是一种溶酶体半胱氨酸蛋白酶,主要表达于中性粒细胞、肥大细胞、巨噬细胞、上皮细胞等,其核心功能是激活一系列与炎症密切相关的丝氨酸蛋白酶,包括中性粒细胞弹性蛋白酶(NE)、组织蛋白酶G(CatG)、蛋白酶3(PR3)和肥大细胞糜酶(Chymase)等,是免疫细胞毒性与炎症启动的核心上游调控因子[1]。
CTSC通过切除这些酶原N末端的二肽片段,使其转化为具有活性的成熟酶形式。因此,CTSC被视为免疫相关丝氨酸蛋白酶的“共同激活通路”。当机体受到感染、损伤、肿瘤微环境刺激时,CTSC会异常高表达,导致大量活性蛋白酶释放,进而引发组织重塑、黏液分泌亢进、免疫细胞浸润等炎症反应,成为多种疾病的共同致病节点。
半胱氨酸蛋白酶在各种炎症性疾病中的作用
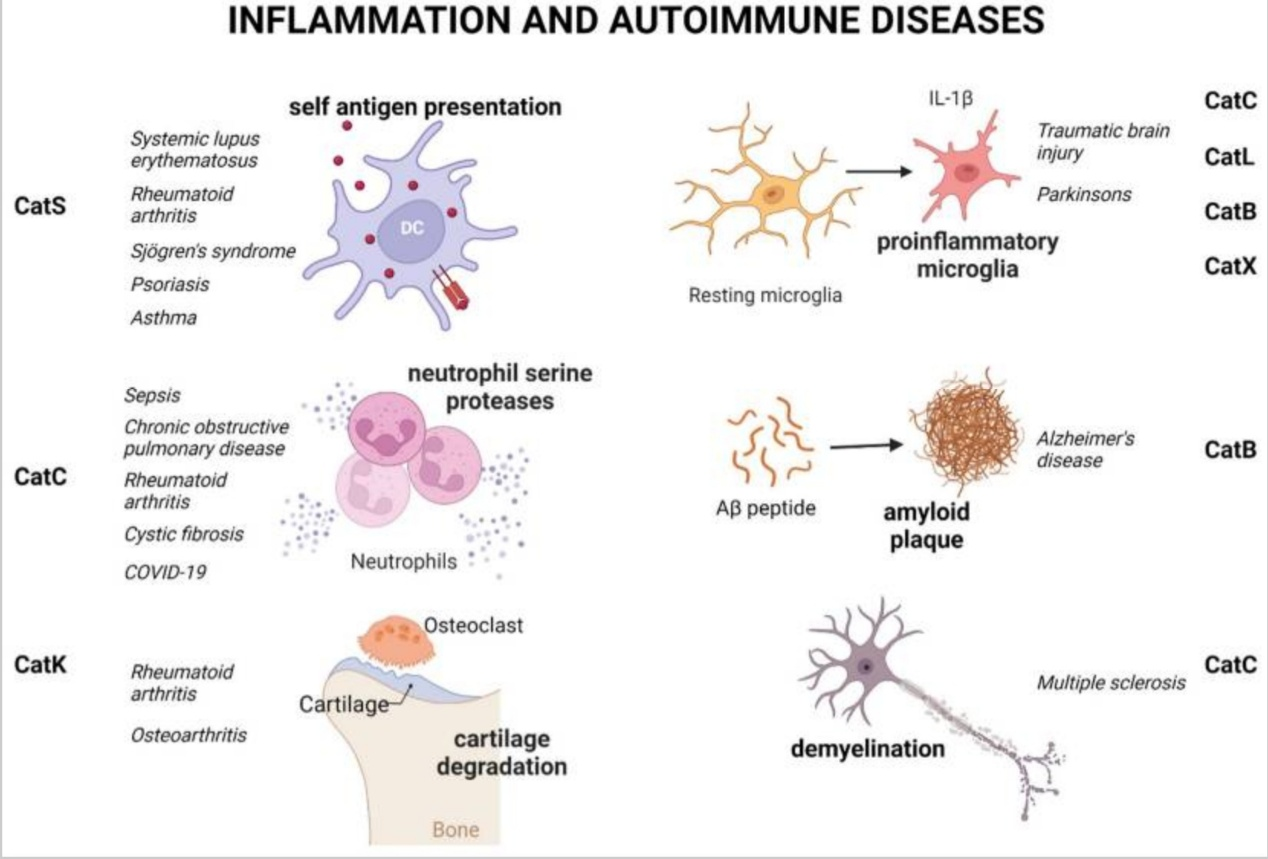
图片来源:文献资料[2]
作为免疫激活与组织重塑的交汇点,CTSC的异常表达与多种疾病进展密切相关,覆盖呼吸疾病、肿瘤转移、免疫与炎症等多个领域。
CTSC在非囊性纤维化支气管扩张(NCFB)、慢性阻塞性肺病(COPD)、哮喘中扮演核心角色。在支气管扩张症中,中性粒细胞来源的NE和PR3过度活跃,驱动中性粒细胞浸润与蛋白酶失衡,导致气道弹性纤维降解、黏液清除障碍和反复感染,形成“炎症-感染-组织损伤”恶性循环;传统抗炎、支气管扩张剂难以阻断蛋白酶介导的组织损伤,成为难治性呼吸疾病的治疗瓶颈。在COPD中,CTSC介导的蛋白酶活性增强同样是肺气肿和慢性支气管炎的重要驱动因素[1]。
CTSC是肿瘤肺转移的关键驱动因子,尤其在三阴性乳腺癌中作用突出。CTSC招募中性粒细胞浸润肺部,诱导中性粒细胞胞外陷阱(NETs)形成,为肿瘤细胞定植提供 “土壤”,促进侵袭与远处转移;高表达CTSC的乳腺癌患者,术后肺转移风险显著升高。在肺癌、结直肠癌等实体瘤中,CTSC同样通过降解基质、激活炎症、重塑微环境,推动侵袭与耐药[3]。
CTSC促进乳腺癌肺转移
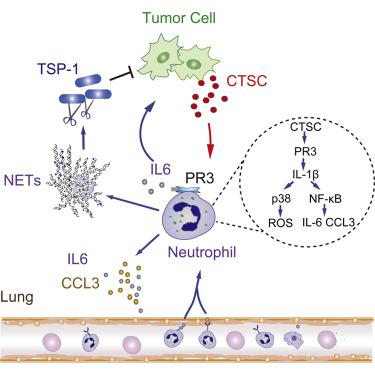
图片来源:文献资料[3]
CTSC通过激活中性粒细胞弹性蛋白酶(NE)、蛋白酶3(PR3)和组织蛋白酶G等关键效应分子,在多种自身免疫和炎症性疾病的病理进程中发挥核心驱动作用。如在牙周炎中,CTSC的高表达与上皮分化功能的改变及TLR4信号通路的激活相关,参与了牙周组织的免疫应答和炎症损伤过程。CTSC基因的纯合突变还可导致Papillon-Lefevre综合征和Haim-Munk综合征,以掌跖角化病和早发性牙周炎为特征。此外,CTSC还在银屑病、炎症性肠病等自免疾病中扮演重要角色。
机制分野:
可逆 vs 不可逆,CTSC抑制剂两大技术路线大比拼
基于CTSC在炎症通路中的上游调控作用,CTSC抑制剂通过与CTSC活性位点可逆结合,竞争性抑制其酶活性,从源头减少中性粒细胞弹性蛋白酶(NE)、蛋白酶3(PR3)、组织蛋白酶G(CatG)和肥大细胞糜酶等多种炎症相关蛋白酶的成熟与释放,从而实现广谱抗炎效果。根据作用机制与结合方式,CTSC抑制剂主要分为以下两类技术路线:
可逆性抑制剂:通过与CTSC活性位点可逆结合,竞争性抑制其酶活性,抑制程度随药物浓度降低而减弱。这类药物的核心优势在于具备良好的安全性窗口和可控的药代动力学特征,适合长期慢性病治疗,可有效避免因过度抑制免疫系统而引发的感染风险。
布索卡替是当前最具代表性的可逆性口服CTSC抑制剂,由Insmed公司原研、阿斯利康参与早期开发,通过对CTSC的可逆性抑制,从源头阻断多种中性粒细胞丝氨酸蛋白酶的激活。目前布索卡替是全球唯一获批上市的CTSC靶向药物,标志着该靶点临床转化的里程碑式突破。
不可逆性抑制剂:通过与CTSC活性位点形成共价键,永久性失活该酶。这类药物理论上具有更强的抑制活性和更持久的药效,但过度抑制免疫功能可能增加感染风险。
GSK-2793660是这一路径的代表分子,由葛兰素史克开发,是一种口服、不可逆的CTSC抑制剂,早期曾被用于支气管扩张症、ANCA相关性血管炎和囊性纤维化等适应症的临床探索。然而,GSK-2793660的I期临床研究结果显示,尽管连续21天每日给药12mg可实现≥90%的CTSC抑制,但下游NE、CatG和PR3的酶活性仅降低约20%,提示该分子存在“中枢抑制强、末端效应弱”的通路局限性;更为关键的是,10名受试者中有7人在给药开始7—10天后出现了手掌和足底的表皮脱屑不良事件,其表现与CTSC基因缺陷患者的部分表型特征相似。这些安全性信号和药效局限性导致该分子的后续开发受阻,也提示不可逆抑制剂在靶点选择性和长期安全性方面,面临更高的研发门槛。
全球研发与临床研究进展:
从零的突破到多元布局
据“药智数据”显示,目前全球CTSC抑制剂以小分子口服药物为主,均为可逆性抑制剂,多条管线进入临床Ⅱ/Ⅲ期,适应症集中于呼吸系统疾病领域。布索卡替是目前全球唯一获批上市的CTSC抑制剂。
布索卡替(Brensocatib,商品名:Brinsupri)是由Insmed公司研发的全球首创、口服、选择性、可逆性CTSC抑制剂。布索卡替通过抑制DPP1活性,阻断中性粒细胞在骨髓成熟过程中激活中性粒细胞丝氨酸蛋白酶(NSPs),进而减少中性粒细胞弹性蛋白酶等炎性因子的释放,从上游调控中性粒细胞介导的炎症反应,是目前唯一获批专门用于治疗非囊性纤维化支气管扩张症(NCFB)的靶向药物,同时布局慢性鼻窦炎、囊性纤维化、化脓性汗腺炎等中性粒细胞介导的炎症性疾病。
关键Ⅲ期ASPEN研究结果显示,与安慰剂相比,每日口服10mg和25mg布索卡替的患者年化肺部急性发作率分别降低21.1%和19.4%,均达到统计学显著差异(P<0.01);10mg组和25mg组首次发作时间均显著延迟,一年内无急性发作的患者比例分别达48.5%和48.5%,而安慰剂组为40.3%;25mg组患者在第52周时肺功能下降亦显著减缓。安全性方面,布索卡替整体耐受性良好,不良事件多为轻至中度[4]。2020年6月,该药获FDA突破性疗法认定;2025年2月NDA获受理并授予优先审评;2025年8月12日正式获FDA批准上市,成为全球首个且唯一获批治疗NCFB的药物。
表 全球上市及临床在研CTSC靶向药
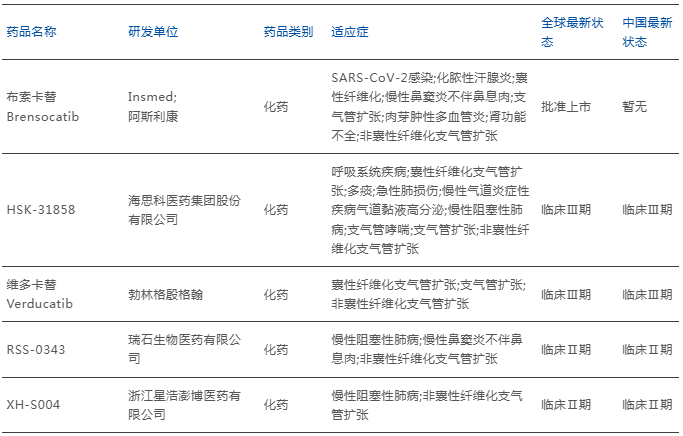
来源:药智数据
目前进入临床研究的管线中,勃林格殷格翰的维多卡替临床研究已推进至Ⅲ期,海思科、瑞石生物、复星医药的国产创新药管线快速跟进,形成与国际前沿并跑格局。
维多卡替(Verducatib)是勃林格殷格翰自主研发的口服、高选择性CTSC抑制剂,核心适应症与布索卡替同为非囊性纤维化支气管扩张症(NCFB)。关键Ⅱ期AIRLEAF研究显示,维多卡替可降低肺部急性加重风险约30%,存在显著剂量依赖性获益,安全性良好。2025年6月维多卡替获FDA突破性疗法认定,全球Ⅲ期研究已启动,中国进口上市申请于2026年1月获得NMPA受理,中国上市进程同步推进。
HSK-31858是海思科自主研发的口服、强效高选择性CTSC抑制剂,核心适应症为NCFB。HSK-31858的关键Ⅱ期SAVE-BE研究显示,每日口服20mg和40mg可使年度病情加重风险分别降低48%和59%,安全性良好。目前NCFB适应症已进入中国Ⅲ期临床,获得CDE突破性治疗认定,针对COPD和哮喘及针对气道黏液高分泌的Ⅱ期临床研究正在同步推进中。2023年11月,海思科将HSK31858大中华区以外全球权益授权给意大利Chiesi集团,获得1300万美元首付款及最高4.62亿美元里程碑付款。
RSS-0343是恒瑞医药自主研发的口服、高选择性CTSC小分子抑制剂,核心适应症为NCFB,同时布局COPD和哮喘。I期临床显示,该药在健康受试者中安全性及耐受性良好,不良事件多为轻中度,药代动力学特征支持后续开发。目前,RSS-0343针对NCFB已进入中国Ⅱ期临床,针对COPD和哮喘的I期研究同步推进。
XH-S004是复星医药控股子公司星浩澎博自主研发的口服、强效高选择性CTSC小分子抑制剂,核心适应症为COPD和NCFB。Ib期临床显示,XH-S004在中重度COPD患者中连续给药140天,耐受性良好,不良事件多为轻中度,肺功能指标有改善趋势。目前,XH-S004针对NCFB已进入中国Ⅱ期临床,针对COPD的Ib期已完成入组。
未来创新方向:
适应症外延、联合策略与前沿技术探索
尽管CTSC抑制剂在临床研究中展现出广阔前景,但其研发仍面临多重挑战。随着可逆性抑制剂成为临床开发的核心路径,不可逆技术路线因安全性风险逐渐边缘化,CTSC抑制剂也衍生出差异化的创新趋势。
目前进入临床研究的CTSC抑制剂均以NCFB作为核心适应症。作为罕见病,NCFB的患者群体相对有限,CTSC抑制剂面临管线同质化的风险。此外,口服给药带来的便利性是CTSC抑制剂相较于注射类生物制剂的显著优势,有助于提升患者依从性。但如何在保证药效的同时实现每日一次或更少频次的给药方案,仍是制剂优化的重要方向。
适应症从罕见病向常见慢性病扩展的趋势已经显现。海思科的HSK31858以NCFB为核心适应症率先进入中国III期临床,并获得CDE突破性治疗认定的同时,同步推进COPD、哮喘和气道黏液高分泌的II期临床,还布局了急性肺损伤等适应症。此外,多条国内管线的COPD和哮喘适应症也已推进至临床研究阶段。尽管COPD等大规模适应症面临疗效终点复杂、研发周期长的挑战,适应症外延仍将是CTSC抑制剂的主要创新方向。
CTSC抑制剂的联合治疗策略目前处于早期探索阶段,未来有望成为CTSC抑制剂临床开发与差异化布局的重要补充路径。CTSC抑制剂从炎症源头阻断蛋白酶级联激活,而抗生素、黏液溶解剂等传统对症药物则在感染控制和症状缓解层面发挥作用,两者协同有望形成“源头阻断+对症清除”的完整治疗链。健康元在支气管扩张症领域的布局中,其妥布霉素吸入液控制感染,而CTSC抑制剂从炎症源头阻断疾病进展,两者共同构成了从“对症”到“病因”的完整治疗链路。目前健康元的CTSC抑制剂项目正式进入PCC(临床前候选药物)阶段,已完成走向临床试验的关键步骤。
靶向蛋白降解嵌合体(PROTAC)利用细胞自身的泛素-蛋白酶体系统,能够靶向传统小分子难以作用的“不可成药”蛋白,克服因突变导致的药物耐药,并凭借催化降解机制实现更低剂量下的持续药效。对于CTSC这一具有不可逆抑制剂安全性风险历史的靶点而言,PROTAC提供了一种全新的干预思路:通过可逆性的催化降解取代不可逆的共价结合,有望在保持强效活性的同时规避长期抑制带来的安全性隐患。目前,针对STING、IRAK4等炎症关键蛋白的PROTAC分子已进入临床或临床前阶段,尽管尚未有针对CTSC的PROTAC管线公开,但该技术为CTSC靶向药从“抑制”走向“降解”的路径转向提供了中长期技术储备。
小 结
CTSC作为炎症与组织重塑的上游总控蛋白酶,其成药突破是广谱抗炎、源头治疗理念的重要落地标志。可逆性抑制剂凭借更优安全窗口成为主流,布索卡替的上市验证了靶点价值,维多卡替、海思科HSK-31858、瑞石RSS-0343、复星XH-S004等国产管线快速推进,形成与国际并跑的创新格局。
尽管当前仍面临适应症集中、疗效终点复杂、给药频次优化等挑战,但联合治疗与PROTAC降解技术有望成为未来开辟差异化空间的路径。未来,CTSC抑制剂有望从非囊性纤维化支气管扩张,逐步拓展至COPD、哮喘、化脓性汗腺炎、肿瘤转移等更多中性粒细胞驱动疾病,成为横跨多个领域的广谱重磅靶点,为长期缺乏有效对因治疗的顽疾带来革命性解决方案。
参考文献:
1.Korkmaz, Brice et al. “Therapeutic targeting of cathepsin C: from pathophysiology to treatment.” Pharmacology & therapeutics vol. 190 (2018): 202-236.
2.Senjor, Emanuela et al. “Cysteine Cathepsins as Therapeutic Targets in Immune Regulation and Immune Disorders.” Biomedicines 11 (2023): n. pag.
3.Xiao, Yansen et al. “Cathepsin C promotes breast cancer lung metastasis by modulating neutrophil infiltration and neutrophil extracellular trap formation.” Cancer cell (2020): n. pag.
4.Haworth, Charles, et al. “Phase 3 Trial of the DPP-1 Inhibitor Brensocatib in Bronchiectasis.” New England Journal of Medicine, vol. 392, no. 16, Apr. 2025, pp. 1569–81,