

布鲁顿酪氨酸激酶(BTK)作为B细胞受体信号通路的关键节点,已成为血液肿瘤与自身免疫性疾病治疗的核心靶点。而共价BTK抑制剂的问世更是为B细胞恶性肿瘤治疗带来革命性突破,但耐药问题(尤其是C481位点突变)及脱靶效应引发的安全性隐患,限制了其长期临床价值。
在此情况之下,临床上除了寄希望于更多全新机制的创新药之外,对于BTK抑制剂的探索也同样并未停止,2025年,非共价BTK抑制剂(ncBTKi)领域更是迎来里程碑式进展:
一者,12月9日美国血液学会(ASH)年会公布的一系列关于非共价BTK抑制剂的重磅临床数据,印证了其在慢性淋巴细胞白血病(CLL)中的卓越疗效。
二者,12月7日国家医保目录首次将全球首个非共价BTK抑制匹妥布替尼纳入报销范围,大幅提升了创新药物的可及性。
更值得关注的是,这类药物凭借独特的作用机制,正突破惰性B细胞淋巴瘤的治疗边界,在侵袭性淋巴瘤与多发性硬化症(MS)等领域展现出巨大应用潜力,开启了靶向治疗的全新篇章。
医保准入破局:
非共价BTK抑制剂临床可及性的历史性跨越
药物可及性作为创新疗法惠及患者的关键一环,是创新价值转化为患者实际获益的重要桥梁。
2025年12月7日,国家医保局发布的新版药品目录传来重磅消息——全球首个非共价BTK抑制“匹妥布替尼(Pirtobrutinib)”成功纳入基本医保支付范围,成为医保目录中首个获批的非共价BTK抑制剂。这一政策红利的释放,不仅是医保支持创新药的重要体现,更对临床治疗格局产生深远影响。
从临床需求来看,对于此前共价BTK抑制剂治疗失败后的套细胞淋巴瘤(MCL)患者而言,如果说,之前产品的获批有效缓解了治疗手段匮乏的困境,那么此次匹妥布替尼的医保准入,一定程度上就为这类难治性患者提供了更为标准化的治疗选择。
从患者负担角度而言,非共价BTK抑制剂作为创新靶向药物,此前高昂的治疗费用让多数患者望而却步。纳入医保后,患者自付比例显著降低,药物可及性得到质的提升,真正实现了“好药进医保,患者用得起”的目标。
从行业发展视角来看,医保政策对匹妥布替尼的认可,一方面将使非共价BTK抑制剂的市场占有率大幅提升,另一方面或许也将进一步激励企业加大非共价BTK抑制剂领域的研发投入,推动其适应症向更多疾病领域拓展,为后续创新药物的临床转化奠定坚实基础。
机制革新:
破解耐药难题,优化临床治疗体验
论及非共价BTK抑制剂的核心优势,应主要源于其独特的作用机制,这也是疗法能够突破共价抑制剂治疗瓶颈的关键所在。
与共价BTK抑制剂通过不可逆结合BTK活性位点(C481残基)发挥作用不同,非共价BTK抑制剂采用可逆性结合方式,无需依赖C481位点,既能有效抑制野生型BTK,又能覆盖C481突变型BTK,从根本上解决了共价抑制剂治疗中最常见的C481突变耐药问题。
以首个获批的非共价BTK抑制剂匹妥布替尼为例,其药代动力学特征经过精准优化,展现出显著优于传统药物的临床特性:
其一,生物利用度高达85.5%,意味着药物口服后能快速且稳定地被机体吸收,确保血药浓度维持在有效治疗水平。
其二,半衰期长达约19小时,支持每日一次口服给药,大幅简化了治疗方案,显著提升了患者的用药依从性。
其三,脱靶效应更低,对其他酪氨酸激酶的抑制作用较弱,为后续安全性优势的展现提供了机制保障。
这种“克服耐药+优化药代动力学”的双重优势,不仅在CLL治疗中得到充分验证,更为其跨疾病领域的应用提供了坚实的结构基础和临床可能性。
ASH 2025重磅数据:
非共价BTK抑制剂重塑CLL治疗格局
2025年ASH年会上,多项关于“匹妥布替尼”治疗CLL的III期临床研究结果公布,以确凿的数据证明了非共价BTK抑制剂在CLL治疗中的核心地位,从一线治疗到耐药后挽救治疗,从单药应用到联合方案探索,全面覆盖了CLL治疗的全周期,彻底重塑了CLL的治疗格局。
一线治疗突破:单药疗效显著优于传统化疗免疫方案
12月9日,礼来在ASH2025大会上首次公布了匹妥布替尼(Pirtobrutinib)对比苯达莫司汀联合利妥昔单抗(BR)治疗初治CLL/SLL患者的Ⅲ期BRUIN CLL-313研究结果。
值得注意的,该临床研究不仅是全球首个评估非共价抑制剂用于初治CLL/SLL患者的Ⅲ期结果,且被ASH大会评为六大突破性摘要(LBA报告),研究结果令人振奋:
在PFS方面,匹妥布替尼组患者的疾病进展或死亡风险显著降低约80%(HR=0.199,p<0.0001),24个月PFS率高达93.4%,而BR方案组仅为70.7%。
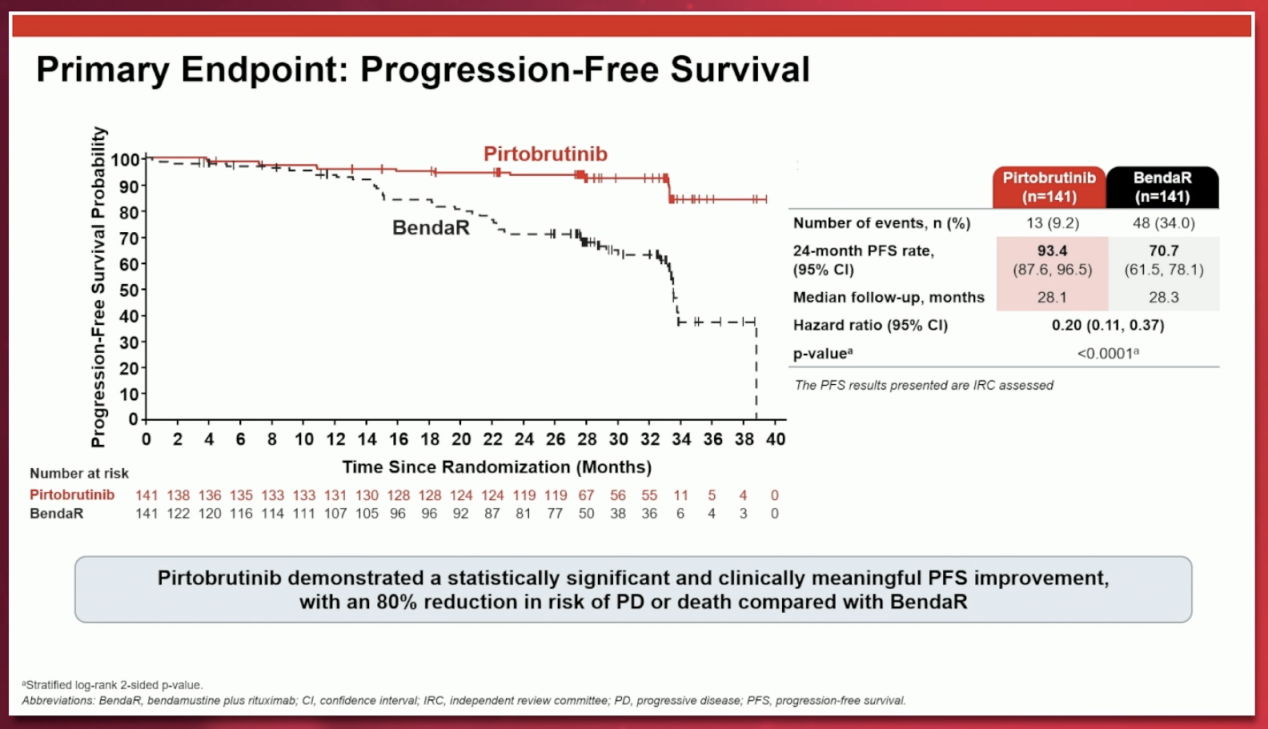
图片来源:丁香园血液时间
客观缓解率(ORR)方面,匹妥布替尼组达到94.3%,远超BR方案组的80.9%。总生存期(OS)方面,匹妥布替尼组展现出明显的获益趋势,死亡风险降低74.3%(HR=0.257,p=0.0261)。
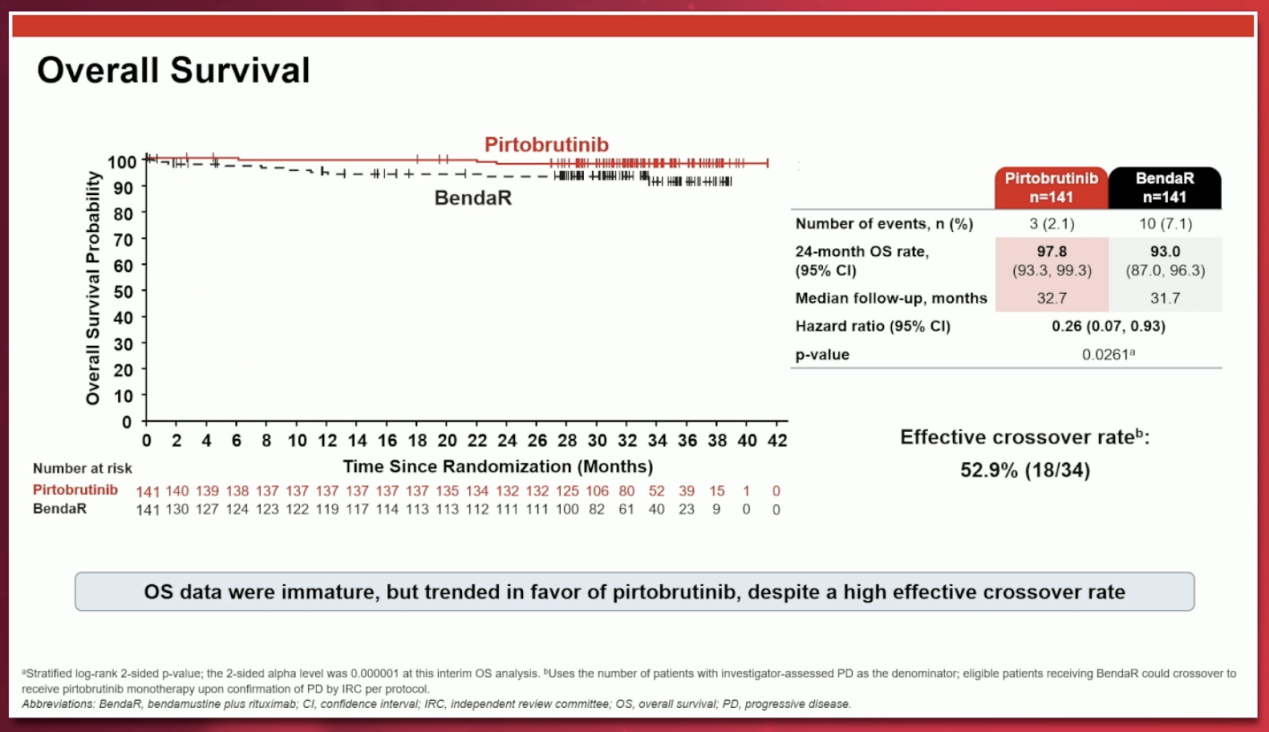
图片来源:丁香园血液时间
而比之有效性更令人兴奋的是,该项关于“非共价BTK抑制剂”的临床研究在安全性方面的优势尤为突出:匹妥布替尼组≥3级不良事件发生率仅为40.0%,远低于BR方案组的67.4%,其中房颤发生率仅为1.4%,显著低于传统方案及部分共价BTK抑制剂。
总的来说,BRUIN CLL-313研究显示,尽管疗法OS数据尚不成熟,但匹妥布替尼在初治CLL/SLL患者中显著改善IRC评估的PFS,其治疗效应为单药BTK抑制剂与BR方案对比中观察到的最大获益之一。同时,匹妥布替尼耐受性良好,安全性特征与已知情况一致,这些数据表明,匹妥布替尼有望成为初治CLL/SLL患者(包括可能仅接受一线治疗的老年患者)的潜在新标准治疗方案。
头对头较量:彰显非共价抑制剂的疗效与安全性优势
在此次ASH2025大会上,除了压轴出场的BRUIN CLL-313研究结果外,关于“匹妥布替尼”也有不少其他重磅研究结果得以公布。
12月8日,美国俄亥俄州立大学的Jennifer A Woyach为带来了全球首个非共价与共价BTK抑制剂头对头比较的III期临床试验,直接对比了匹妥布替尼与伊布替尼在BTK抑制剂初治(BTKi-naïve)CLL患者中的表现(BRUIN CLL-314研究--NCT05254743)。
研究结果显示,在ORR方面,匹妥布替尼组不仅达到非劣效性终点,更展现出数值上的优势:
意向治疗(ITT)人群中ORR为87.0% vs 78.5%,其中一线治疗人群ORR高达92.9% vs 85.8%。
PFS方面,匹妥布替尼组展现出显著的获益趋势,一线治疗人群疾病进展或死亡风险降低76%(HR=0.24),18个月PFS率为95.3% vs 87.6%。
安全性方面,匹妥布替尼组的优势更为显著,房颤发生率仅为2.4%,远低于伊布替尼组的13.5%,高血压发生率也更低(10.6% vs 15.1%)。
这一研究结果不仅验证了非共价BTK抑制剂的疗效不劣于甚至优于经典共价抑制剂,更凸显了其在安全性上的独特优势,为临床治疗方案的选择提供了更优解。
耐药后挽救:填补共价抑制剂失败后的治疗空白
正如前文所讲,对于共价BTK抑制剂治疗失败的复发/难治性(R/R)CLL患者,其治疗选择极其有限,预后极差。

图片来源:JCO杂志截图
在之前JCO杂志上,礼来公布了匹妥布替尼对于耐药人群的BRUIN CLL-321研究(NCT04666038)结果,该实验对比了匹妥布替尼单药与Idelalisib+利妥昔单抗或BR方案的疗效。
研究结果显示,匹妥布替尼组患者的中位PFS达到14.0个月,显著长于对照组的8.7个月(HR=0.54);至下一次治疗时间(TTNT)方面,匹妥布替尼组长达24.0个月,是对照组(10.9个月)的2倍多(HR=0.37)。
安全性方面,匹妥布替尼组≥3级治疗相关不良事件(TEAE)发生率为57.7%,显著低于对照组的73.4%,治疗停药率也更低(17.2% vs 34.9%)。更重要的是,匹妥布替尼组在研究期间未观察到Richter转化(CLL转化为侵袭性淋巴瘤),而Richter转化是CLL患者预后不良的重要标志。
更值得注意的是,2025年12月3日,美国食品药品监督管理局(FDA)已授予匹妥布替尼传统批准,用于治疗既往接受过共价布鲁顿酪氨酸激酶(BTK)抑制剂治疗的复发或难治性慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)成人患者。
一系列数据表明,匹妥布替尼为共价BTK抑制剂治疗失败的R/R CLL患者提供了有效的挽救治疗方案,填补了临床治疗的重要空白。
联合方案探索:迈向CLL功能性治愈的新方向
微小残留病(MRD)阴性是CLL治疗追求的重要目标,也是实现疾病长期控制甚至治愈的关键指标。
NCT05536349研究作为一项II期临床试验,探索了匹妥布替尼联合维奈克拉+奥法木单抗方案在一线CLL患者中的疗效与安全性。
研究结果展现出令人惊喜的疗效:治疗第13周期时,血液中无法检测到MRD(U-MRD4)的患者比例达到100%,骨髓中U-MRD4阴性率达到97%;更值得关注的是,患者在完成固定周期治疗停药后,中位8.6个月内未出现MRD复发。安全性方面,联合方案未出现新增的严重不良事件,耐受性良好。
这一研究结果表明,非共价BTK抑制剂联合其他靶向药物的方案,有望实现CLL患者的深度缓解乃至功能性治愈,为CLL治疗开辟了全新的方向。
拓展侵袭性淋巴瘤:
DLBCL治疗的新希望
弥漫大B细胞淋巴瘤(DLBCL)作为最常见的侵袭性B细胞淋巴瘤,虽然部分患者可通过标准治疗治愈,但复发/难治性DLBCL患者的预后依然极差,5年生存率不足10%,临床需求迫切。
非共价BTK抑制剂凭借其独特的机制优势,在DLBCL治疗中展现出巨大的潜力,多款药物已进入临床研究阶段,为这类患者带来了新的希望。
洛布替尼(LP-168):双重机制引领DLBCL治疗突破
洛布替尼是全球首个兼具共价不可逆与非共价可逆双重作用机制的BTK抑制剂,这种独特的设计使其既能强效抑制野生型BTK,又能有效克服C481突变耐药,同时对BTK的抑制作用更持久、更稳定。
其I期临床研究结果在R/R非生发中心B细胞样(non-GCB)DLBCL患者中展现出优异的疗效:ORR达到57.8%,完全缓解(CR)率为31.3%;对于接受过三线及以上治疗的患者,ORR仍高达68.8%,CR率为43.8%;中位PFS为7.1个月,12个月PFS率达到48.7%。
安全性方面,≥3级治疗相关不良事件(TRAE)发生率仅为40%,未出现因TRAE导致的治疗停药或死亡病例,耐受性良好。
基于这一优异的临床数据,洛布替尼于2024年获得国家药品监督管理局药品审评中心(CDE)突破性治疗认定,目前其II期注册研究(ROCK-2)已正式启动,有望加速其在DLBCL治疗中的临床应用。
HMPL-760:高选择性非共价抑制剂的联合治疗探索
HMPL-760是一款高度选择性的非共价BTK抑制剂,通过可逆性结合BTK活性位点,高效抑制BTK信号通路,同时能有效克服C481S突变耐药。
其I期临床研究(NCT05190068)纳入了26例R/R B细胞非霍奇金淋巴瘤(B-NHL)患者,结果显示ORR达到73.1%,其中DLBCL患者也观察到明确的CR和部分缓解(PR);在既往接受过BTK抑制剂治疗失败的患者中,ORR更是高达87.5%,充分验证了其克服耐药的能力。研究同时确定了其推荐II期剂量(RP2D)为400mg每日一次口服,安全性良好。
目前,HMPL-760的III期临床研究(CTR20254776)已正式开展,该研究采用HMPL-760联合R-GemOx方案(利妥昔单抗+吉西他滨+奥沙利铂)对比安慰剂联合R-GemOx方案,目标入组240例患者,主要研究终点为PFS,次要终点包括OS、ORR、缓解持续时间(DOR)等。
该研究的开展旨在探索非共价BTK抑制剂联合化疗免疫方案在DLBCL治疗中的价值,有望将其治疗地位前移至二线甚至一线,为改善高危DLBCL患者的预后提供新的治疗策略。
跨界免疫疾病:
开启多发性硬化症治疗的新纪元
当然,除了血液肿瘤领域,非共价BTK抑制剂凭借其免疫调节作用,在自身免疫性疾病治疗中也同样展现出巨大的潜力。
其中,多发性硬化症(MS)作为一种中枢神经系统慢性炎症性脱髓鞘疾病,其发病机制与B细胞异常活化密切相关,目前临床治疗药物虽能部分控制疾病进展,但仍存在未被满足的需求。而非共价BTK抑制剂通过抑制B细胞和髓系细胞的信号通路,兼具免疫调节与神经保护双重作用,为MS治疗带来了全新的突破,其中罗氏公司的Fenebrutinib表现最为突出。
Fenebrutinib作为一款高选择性的非共价BTK抑制剂,通过精准抑制BTK信号通路,有效调控B细胞的活化、增殖与分化,同时抑制髓系细胞的促炎反应,从而减轻中枢神经系统的炎症损伤;此外,研究发现其还具有神经保护作用,能够减少脱髓鞘病变和轴索损伤,延缓疾病进展。
其一系列关键III期临床研究结果展现出优异的疗效:在复发型MS患者中开展的FENhance 1 & 2研究(NCT04586023)显示,Fenebrutinib治疗组患者的年复发率(ARR)显著降低,MRI病灶活动几乎完全被抑制,残疾恶化风险也得到显著降低;在原发进展型MS患者中开展的FENtrepid研究(NCT04544449)显示,Fenebrutinib在降低确认残疾进展(CDP)风险方面与现有标准治疗药物奥法木单抗相当,同时显著减少MRI病灶活动;长期随访研究(NCT04586010)进一步验证了其疗效的持续性,患者疾病活动得到长期抑制,复发率维持在较低水平,且安全性良好,未出现新增的严重不良事件。
作为首个在复发型和进展型MS中均展现出积极结果的BTK抑制剂,Fenebrutinib的临床研究结果具有里程碑意义,其开启了MS治疗“免疫调节+神经保护”双重作用的新纪元,为MS患者提供了更有效的治疗选择,有望重塑MS的治疗格局。
结语与展望
以目前非共价BTK抑制剂所表现出的应用趋势来看,凭借其独特的可逆性结合机制,已成功破解了共价BTK抑制剂面临的耐药难题,同时通过优化的药代动力学特征,显著提升了临床治疗的安全性与依从性。
而企业层面,非共价BTK作为第三代BTK技术很大程度上对替代传统BTK有着替代趋势,现阶段传统BTK抑制剂的头部玩家,也均有不同程度的布局力度,除此之外,后续还有BTK PROTAC在研(如BGB16673),以及更多候选药物的临床推进。
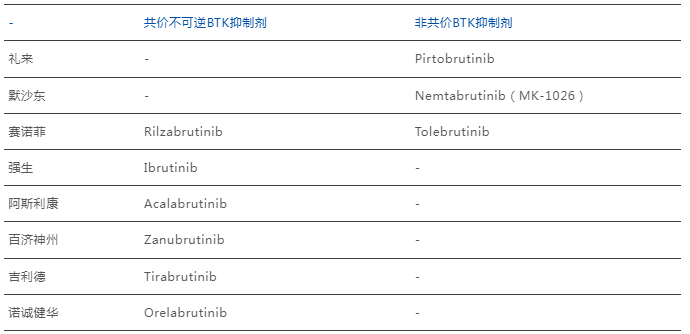
数据来源:药智数据、公开数据整理
2025年无疑是非共价BTK抑制剂领域的“里程碑之年”——医保准入实现临床可及性的历史性跨越,ASH年会重磅数据确立其在CLL治疗中的核心地位,机制革新破解了共价抑制剂的耐药与安全性痛点,更在侵袭性淋巴瘤与多发性硬化症等领域完成了突破性拓展。从慢性淋巴细胞白血病的一线治疗到耐药后挽救,从弥漫大B细胞淋巴瘤的难治性患者救治到多发性硬化症的“免疫调节 + 神经保护”双重突破,非共价BTK 抑制剂以独特的可逆结合机制为支点,不仅填补了多项临床治疗空白,更重塑了多个疾病领域的治疗格局。
匹妥布替尼的医保落地让创新药惠及更多患者,洛布替尼、HMPL-760在侵袭性淋巴瘤的临床进展,以及Fenebrutinib在MS领域的革命性突破,共同印证了这类药物 “超越单一疾病”的广阔应用前景。
未来,随着联合治疗方案的深入探索、适应症的持续拓展;就分子结构而言,目前除了ncBTK,后续还有BTK PROTAC在研(如BGB16673),以及更多候选药物的临床推进,新一代BTK抑制剂将持续打破治疗边界,为血液肿瘤与自身免疫病患者带来更精准、更安全、更可及的治疗选择,推动靶向治疗进入“耐药可控、跨界可及”的全新阶段。